再生医療の定期報告|費用の内訳と見直しの考え方

再生医療等を提供している医療機関にとって、「定期報告」は運用を継続するうえで必ず対応しなければならない手続きの一つです。
再生医療等提供計画の提出後は、一定期間ごとに実施状況を整理し、定期報告として提出する必要があります。
報告書の様式自体は一見シンプルに見えるものの、委員会ごとの運用差や追加資料への対応が求められるため、実際には医療機関にとって想定以上に負担が生じやすい手続きです。
こうした背景から、再生医療導入のコンサルタントとして、「定期報告」についてご相談をいただく機会も少なくありません。
この記事では、再生医療における定期報告の基本的な仕組みを整理したうえで、手続きにかかる費用の内訳や実務上の負担を踏まえ、コストや運用の見直しを検討する際の考え方について解説します。
定期報告の概要
まずは、再生医療における定期報告の全体像を整理しておきましょう。
再生医療を継続して提供するためには、定期的な報告が義務付けられています。
定期報告には大きく分けて、以下の2種類があります。

特定細胞加工物製造状況の定期報告
特定細胞加工物製造事業者に求められる報告であり、院内で細胞加工を行っている医療機関では対応が必要です。
主な報告内容は、
・製造件数
・苦情の有無
などで、提出期限は受理日から1年と60日以内とされています。
たとえば、受理日が4月1日の場合は、翌年3月31日までの実績をまとめ、5月末までに提出する必要があります。
参考資料(厚生労働省)
再生医療等提供状況の定期報告
実際に提供した再生医療の内容について報告するものです。
主な報告内容は、
・治療を受けた患者数
・有害事象の発生状況
・安全性および科学的妥当性の評価
・患者の経過(改善の有無など)
などです。
報告は、提供計画の受理日から起算して1年間の実施状況を取りまとめ、受理日から1年と90日以内に提出します。
たとえば、受理日が4月1日の場合は、翌年3月31日までの実績をまとめ、6月末までに提出する必要があります。
定期報告の様式や記載要領は、厚生労働省が公開している資料で確認できます。
いずれの報告についても、対象期間内の実施件数が0件であっても報告義務は免除されないことは注意すべき点です。
定期報告の基本的な手続きの流れ
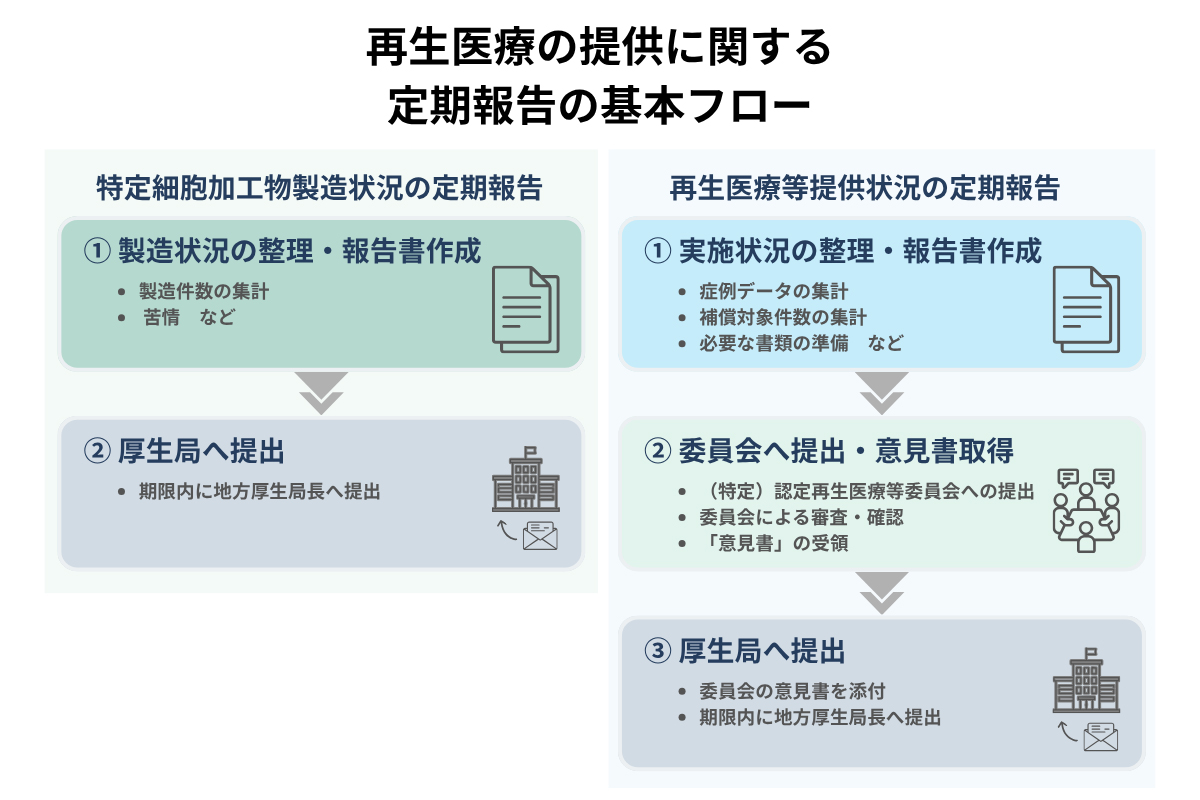
次に、定期報告の基本的な手続きの流れを整理しておきましょう。
定期報告には、「特定細胞加工物製造状況」と「再生医療等提供状況」の2つがあり、それぞれ個別に報告が必要です。ここでは、「再生医療等提供状況」の基本的な手続きの流れを整理します。
手続きは、大きく分けて以下の3つの工程で進みます。
対象期間内の実施状況をまとめます。
報告内容としては、単に実施件数を整理するだけでなく、治療ごとの経過や評価指標の整理が求められる場合があります。また、委員会によっては統計データの提出が必要となる場合もあります。
さらに、近年では行政からの要請により、スタッフへの教育・研修の実施履歴を記録した「教育記録簿」の管理が求められるケースもあります。当センターでは、こうした教育記録簿の整備やスタッフ研修を含めたサポートも行っています。
作成した報告書を特定認定再生医療等委員会(または認定再生医療等委員会)へ提出します。
委員会ごとに確認の観点や求められる資料の粒度が異なるため、過去の提出実績や指摘傾向を踏まえた対応が必要になります。こうした違いを把握していない場合、修正や追加対応が発生し、想定以上に時間や手間がかかる要因となることも少なくありません。
近年では、一部の委員会において、申請方法のばらつきや不備、個別対応の増加を背景に、申請サポート業者や専門家を介した申し込みを前提とする動きも見られます。
そのため、従来のように自己判断で進めるだけでは対応が難しくなるケースもあり、委員会の運用に合わせた体制構築が重要になっています。
委員会の意見書を添えて、期限内に地方厚生局長へ報告書を提出します。
以上の3ステップが、「再生医療等提供状況」の定期報告の基本的な流れです。
続いては、毎年発生するこれらの手続きにかかる費用について、その内訳を整理します。
定期報告の手続きにかかる主な費用
定期報告の運用において発生する費用は、主に外部に支払う費用として大きく次の2つに分けられます。
いずれも毎年発生する費用であるため、運用体制によっては長期的な負担に差が出やすいポイントとなります。

委員会の定期報告審査費
定期報告では、認定再生医療等委員会へ報告を行い、内容の確認および意見を受ける必要があります。
発生する費用は委員会ごとに異なりますが、一般的には10万円〜30万円程度の範囲で設定されているケースが多く見られます。
委員会によっては、追加対応や再提出に伴う費用が設定されている場合もあるため、事前に費用体系を確認しておくことが重要です。
外部サポート費用
定期報告の作成や提出対応を、再生医療の導入支援会社や行政書士などに依頼している場合、別途費用が発生します。
主な業務内容としては、
・定期報告書の作成支援
・委員会提出資料の作成
・修正対応
・厚生局提出のサポート
などが挙げられます。
これらの費用は、年間契約に含まれている場合もあれば、定期報告ごとに個別で発生する場合もあります。また、支援内容や関与範囲によって費用は大きく異なります。
一般的な目安としては、数万円から数十万円程度と幅があり、依頼内容によって差が出やすい領域です。そのため、「どこまでを外部に依頼するか」を整理することが、コスト最適化の観点では重要になります。
定期報告、(特定)認定再生医療等委員会の切り替えはできる?
定期報告の費用についてお話しすると、避けて通れないのが「委員会を変更できないのですか?」というご相談です。
先述のとおり、年に一度、必ず「委員会の定期報告審査費」が必要です。この費用は委員会によってかなりの差があり、実際にいくつかの主要な委員会が公開している審査費用(定期報告分)を比較してみると、その差は一目瞭然です。
| (特定)認定再生医療等委員会の名称 | 一種 | 二種 | 三種 |
|---|---|---|---|
| 日本先進医療臨床研究会(JSCSF) | 320,000円 事務手数料2万円含む | 120,000円 事務手数料2万円含む | 60,000円 事務手数料2万円含む |
| JAMA 日本先進医療医師会 | 220,000円 | ||
| 安全未来 特定再生医療等委員会 | 110,000円 | 110,000円 | 110,000円 |
| ヴィヴィアン 認定再生医療等委員会 | 308,000円 | 308,000円 | 176,000円 |
| JAPSAM 先端医療推進機構 再生医療等委員会 | 330,000円 | 290,000円 | 190,000円 |
| CONCIDE 認定再生医療等委員会 | 220,000円 | 110,000円 | |
| 日本肌再生医学会 認定再生医療等委員会 | 300,000円 | 300,000円 | 200,000円 |
参考:再生医療等安全性確保法第26条第4項の規定により認定された認定再生医療等委員会の一覧より
例えば、第3種の定期報告に関しても5万円程度ですむ委員会もあれば、25万円以上かかる委員会もあるため、あとになって、「委員会を変更したのですが」というご相談を受けることがあります。
結論をお伝えすると、再生医療等の安全性の確保等に関する法律の第三十条の二において、
「提供機関管理者は、法第四条第一項の規定により、再生医療等提供計画を厚生労働大臣に提出した後は、認定再生医療等委員会が廃止された場合その他のやむを得ない事情がある場合を除き、再生医療等提供計画に記載されている認定再生医療等委員会を変更してはならない。」
と定められているため、原則として認定再生医療等委員会を変更することはできません。
つまり、再生医療導入時に選定した認定再生医療等委員会で、継続して定期報告を行う必要があります。
そのため、定期報告にかかるコストを見直す際は、委員会そのものではなく、報告書作成や進行管理などの運用面・支援体制に関するコストを見直すことが、現実的なアプローチとなります。
ただし、「認定再生医療等委員会が廃止された場合その他のやむを得ない事情」がある場合には、変更が認められるケースもあります。
実務上は厳しい条件が伴うため容易ではありませんが、個別の状況によっては対応可能な場合もございます。詳細についてはお気軽にご相談ください。
【関連記事】

まとめ
再生医療の定期報告は、単なるルーティンワークではありません。
年に一度、現在の運用が法令に則っているかを確認するとともに、無駄なコストや手間が発生していないかを見直す重要な機会でもあります。
進め方によっては、必要以上の工数や費用がかかっているケースもあり、運用の見直しによって負担を適正化できる可能性があります。
当センターでは、現在の運用状況を踏まえ、定期報告に関わる業務フローやサポート体制の見直しをご提案しております。
現状の定期報告の運用に少しでも負担や非効率を感じている場合は、一度見直しをご検討ください。
まずはお気軽にご相談いただけますと幸いです。
再生医療のトータルサポートをご提供しています

当センターは、PRP療法・幹細胞治療を中心とした再生医療導入のトータルサポートをご提供しています。
当センターの支援の特長
- (特定)認定再生医療等委員会の選定サポート
条件に合った委員会ご紹介します - あらゆる治療法・疾患の相談可能
まだ全国で申請事例のない治療にも積極的に取り組んでいます - 開業前でも審査可能な委員会をご提案
開業準備中でも申請が可能な委員会を選定し、スムーズな導入をサポートします - 治療レクチャー・院内研修サポート
治療開始前にはデモ会を開催し、医師・スタッフの皆様が安心して導入できるようサポートします - 収支シミュレーション/競合調査付き
治療単価、患者数、地域特性などをふまえ、10年先まで見据えた計画設計をサポート - 申請実績150件超の経験値と対応力
書類の質と経験値が、審査通過のスムーズさに大きく影響します - 全国対応(訪問+WEB)
初回は必ず現地に伺い、状況をふまえたご提案を行っています - 業界最安値帯の価格設定(新規・定期サポートとも)
継続支援も都度対応のため、月額費用などの固定コストは発生しません - 委員会・PRPキット・幹細胞培養委託先の候補提示
選定に迷わないよう、条件に合った候補リストを提示します(最終選定は医療機関側にて) - 導入後も安心の支援体制
定期報告・変更申請はもちろん、院内用のリーフレットやポスターなど販促面もサポートしています
当センターは、将来を見据えた「選ばれるクリニックづくり」を見据えてサポートいたします。
再生医療の導入をご検討中の方は、まずはお気軽にご相談ください。
\お気軽にご連絡ください/